Significado de cuanto/quantum (de energía y luz) Definición, catástrofe ultravioleta, planck y einstein

Licenciada en Física
Definición formal
El quantum es la cantidad mínima en que se puede presentar una magnitud dada, como por ejemplo la carga eléctrica, la energía y el momentum, entre otras.

La idea de que algunas magnitudes físicas se presentan en pequeños paquetes o cuantos dio origen a una nueva rama de la Física: la Física cuántica, que se diferencia de la Física clásica en que, para esta última, la energía y el momentum pueden tomar cualquier valor dentro de un continuo.
Y esta idea de la cuantización surgió porque hay fenómenos que no logran explicarse del todo a través de los postulados de la física clásica, esa que comprende la mecánica newtoniana, la termodinámica y la teoría electromagnética de Maxwell.
Es así que algunos físicos visionarios se percataron, a principios del siglo XX, de que la materia y la luz se comportaban de una cierta manera a escala macroscópica, y de otra forma muy diferente a escala microscópica.
Pero lo cierto es que todos están familiarizados con la cuantización, porque existe una cantidad cuantizada manejada a diario: el dinero.
En cada país hay una cantidad mínima de dinero, llámese céntimos, centésimos o centavos. El nombre cambia, pero, en cualquier caso, es seguro que cualquier monto de dinero se expresa como múltiplos de ella. Esa mínima cantidad es el “cuanto”.
De esta misma forma funciona la cuantización en Física: hay magnitudes con una cantidad mínima, y cualquier cantidad de esa magnitud, viene dada en términos de ella.
La catástrofe ultravioleta
La historia de cómo la Física adoptó el concepto de cuantización tiene lugar a finales del siglo XIX y comienzos del XX. En aquel entonces la experimentación científica mantenía el auge que había comenzado con la revolución industrial, pero los científicos comenzaron a ver resultados inesperados.
Por ejemplo, se creía que cuanto más se calentaba un objeto, mayor era la irradiación de luz, una suposición bastante razonable, pero que no coincidía del todo con la realidad.
Se sabía ya que la radiación depende de la longitud de onda o de la frecuencia, ambas son recíprocas. Ahora bien, un objeto que se calienta, tal como una barra de acero, va cambiando de color, primero llega al rojo (menor frecuencia, mayor longitud de onda) y si se calienta más, se pone al blanco (mayor frecuencia, menor longitud de onda).
Todas estas emisiones luminosas pertenecen al espectro visible, pero calentando aún más la barra, esta debería emitir energía en el rango del ultravioleta, el cual limita con la luz violeta, pero que es invisible al ojo humano. Y, sin embargo, es obvio que el acero no se vuelve invisible por más que se caliente.
La predicción clásica afirma que a mayor calentamiento corresponde más irradiación, así que, en un principio, al tender la longitud de onda a 0, se tendría una irradiación infinita. Así, la barra de acero podría emitir ultravioleta si se calentara lo suficiente.
Este modelo se llama teoría de Rayleigh-Jeans y la radiancia espectral ε en función de la longitud de onda λ es:
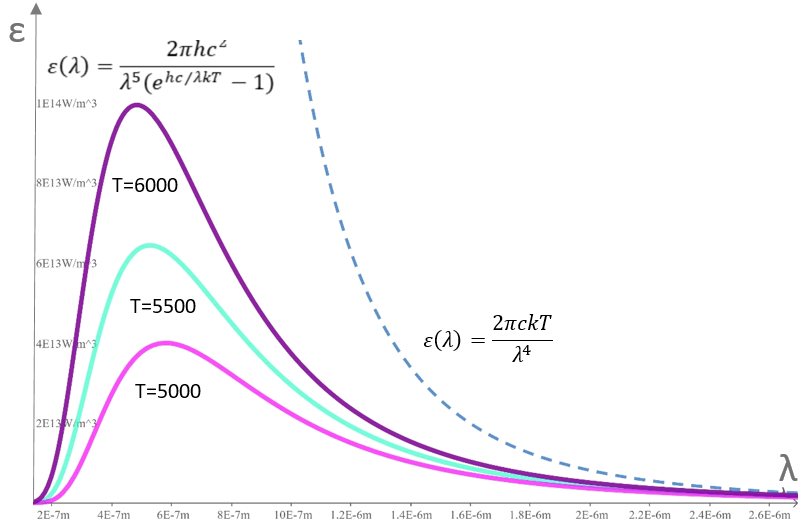
\(\varepsilon \left( \lambda \right)=\frac{2\pi ckT}{{{\lambda }^{4}}}\)
En la gráfica de abajo se muestra la curva (línea segmentada en azul).
Pero la observación experimental coincide con las curvas en línea continua, y de acuerdo a esto, los objetos apenas emiten radiación ultravioleta cuando se calientan (véase el máximo para cada temperatura).
La ley de Rayleigh-Jeans solamente es válida para λ grandes (bajas frecuencias: rojo a infrarrojo). Para los otros valores no se tenía explicación.
Esto se conoce como la catástrofe ultravioleta porque es en este rango que falla la teoría clásica, y era muy catastrófico para los científicos, porque no conseguían averiguar el motivo, por más empeño que ponían.
Características del cuanto de energía
El gobierno alemán había encomendado al físico Max Planck (1858-1947) un estudio para mejorar las bombillas incandescentes. Y por supuesto, al tratar de encontrar la relación entre emisión de luz y la temperatura, Planck se enfrentó a la catástrofe ultravioleta, dilema que luego de algún tiempo resolvió proponiendo una hipótesis revolucionaria:
“La energía se absorbe y se emite en forma de pequeños paquetes llamados cuantos”
Revolucionaria, porque todos suponían que la energía se podía irradiar en cualquier cantidad.
Con esta hipótesis, Planck halló en 1900 una fórmula que concuerda con todos los resultados experimentales, y que tiene a la ley de Rayleigh-Jeans como caso particular. Se conoce como la ley de Planck:
\(\varepsilon \left( \lambda \right)=\frac{2\pi h{{c}^{2}}}{{{\lambda }^{5}}\left( {{e}^{{}^{hc}\!\!\diagup\!\!{}_{\lambda kT}\;}}-1 \right)}\)
Donde:
• h: constante de Planck = 6,626 070 15 × 10-34 J.s
• k: constante de Boltzmann = 1.38 × 10-23 J/K
• c: velocidad de la luz =3 × 108 m/s
Planck la encontró suponiendo una sencilla ecuación para la energía de la radiación:
E = nhf
Donde n es un entero (n = 1, 2, 3…) y f es la frecuencia de la radiación.
Como la constante de Planck es tan pequeña, no es sorprendente que la cuantización de la energía pasara desapercibida durante tanto tiempo.
Características del cuanto de luz
El cuanto de luz se llama fotón y fue propuesto por Albert Einstein (1879-1955) en 1905, partiendo de los resultados de Planck, para explicar el efecto fotoeléctrico descubierto algunos años antes.
En el efecto fotoeléctrico, los electrones emergen de una placa de metal cuando es iluminada con luz visible o luz ultravioleta.
Al explicar el fenómeno, Einstein extendió el concepto de cuantización a todo el espectro electromagnético, no solamente a las regiones visibles y ultravioleta, afirmando que toda onda electromagnética está constituida por fotones de energía E = hf.
Más adelante se demostró experimentalmente que había una relación lineal entre la energía máxima de los electrones que emergían del metal (fotoelectrones) y la frecuencia f de la luz incidente. La pendiente de la recta no es otra que la constante de Planck, quedando así confirmada la teoría de Einstein del efecto fotoeléctrico.
El cuanto de carga
La carga eléctrica libre más pequeña que puede encontrarse en la naturaleza es la del electrón, y su magnitud es de 1,602 x 10-19 C. Se la conoce como la carga elemental, pues cualquier otra carga eléctrica es múltiplo de este valor.
El electrón había sido descubierto previamente por J.J. Thomson (1856-1940) en 1897, pero sin haber determinado el valor numérico de la carga, solo su razón masa/carga.

Trabajo publicado en: May., 2021.
Ilustraciones: pixel