Significado de efecto fotoeléctrico Definición, ejemplos, einstein y el fotón

Licenciada en Física
Definición formal
El efecto fotoeléctrico es el fenómeno que se presenta cuando una superficie metálica o semiconductora produce electrones, al incidir luz sobre la misma, siempre que el espectro de frecuencias de dicha luz esté entre el ultravioleta y el rango visible.
El efecto fotoeléctrico fue descubierto en 1887 por el físico alemán Heinrich Hertz (1857-1894), mientras experimentaba con tubos de descarga eléctrica. Hertz notó que al iluminar uno de los electrodos, entonces la descarga se iniciaba con mayor facilidad, dado que se requería un voltaje menor.
Posteriormente, el físico inglés Joseph J. Thompson descubrió los rayos catódicos en 1899, y sus investigaciones le llevaron a concluir que estos rayos estaban constituidos por partículas de carga negativa, a las que llamó “electrones”. En sus experimentos, Thompson también notó que algo sucedía al iluminar un trozo de metal con luz ultravioleta: emergían electrones.
Ejemplos de aplicación
Desde que fue descubierto hasta la actualidad, al efecto fotoeléctrico se le han encontrado innumerables aplicaciones prácticas entre las que podemos nombrar las siguientes:
– Celdas fotoeléctricas que funcionan como interruptores activados por la luz.
– Celdas fotomultiplicadoras que sirven para detectar luz muy tenue, como la proveniente de las estrellas. Gracias a estas celdas ha sido posible identificar el espectro de su luz y los elementos químicos que conforman a estas estrellas.
– Las primeras cámaras de televisión hacían uso del efecto fotoeléctrico a través de los tubos al vacío que contenían. Estos tubos convertían la luz en señal eléctrica que luego se transmitía a gran distancia.
– Las cámaras digitales y de video actuales también se basan en el efecto fotoeléctrico, solo que los detectores son celdas semiconductoras, en vez de placas metálicas.
Más allá de las aplicaciones prácticas del efecto fotoeléctrico, fue su explicación teórica, dada por Albert Einstein (1879-1955) en 1905 la que inicia la revolución en la Física y dando lugar a una nueva rama: la Física cuántica.
Albert Einstein es famoso por su teoría de la relatividad, pero pocos saben que él no obtuvo el premio Nobel en 1921 por esta teoría, sino por su explicación del efecto fotoeléctrico.
Montaje experimental
En la siguiente figura se muestra el montaje experimental del efecto fotoeléctrico. Consiste en dos electrodos metálicos colocados uno frente al otro en un tubo de vidrio al vacío, esto es necesario para que las moléculas de aire circundante no absorban los electrones desprendidos.
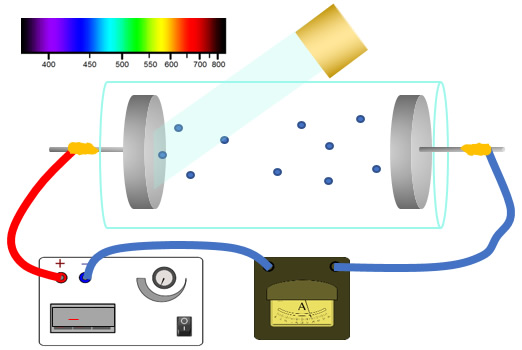
Para estudiar la dependencia del fenómeno, ya sea con la frecuencia o con longitud de onda de la luz incidente, se requiere de una fuente luminosa que provea cada color del espectro. Esto puede hacerse usando una fuente de luz blanca, la cual se dispersa mediante un prisma que la separa en colores. Luego se selecciona el color deseado para iluminar el electrodo, mediante una rendija que sólo permita el paso del mismo.
Sí uno de los electrodos se ilumina con luz de frecuencia suficientemente alta, se desprenden electrones que, si tienen suficiente velocidad, llegan hasta el electrodo opuesto. Así se establece una corriente eléctrica, ya que los electrodos están conectados por un cable externo que cierra el circuito, como se aprecia en la figura.
Adicionalmente, en el circuito exterior se intercalan una fuente de voltaje y un amperímetro. La fuente de voltaje colocada a 0 voltios equivale a un cable, pero los electrones se aceleran estableciendo un voltaje negativo en el electrodo emisor y se frenan cambiando la polaridad. El amperímetro sirve para medir la corriente total del circuito.
La frecuencia umbral
En el estudio del efecto fotoeléctrico se busca establecer la relación entre la emisión de fotoelectrones y la frecuencia de la luz aplicada a la superficie del electrodo metálico.
Uno de los hallazgos más sorprendentes es que, para un metal dado, el fenómeno ocurre solamente si la frecuencia de la radiación aplicada está por encima de cierto valor mínimo, denominado “frecuencia umbral”.
La frecuencia umbral depende del metal utilizado, por ejemplo, para el sodio es 551 Tera hertzios (correspondiente a una longitud de onda de 544 nanómetros). Esto significa que el fenómeno de emisión de electrones se presenta únicamente si la frecuencia luminosa está por encima de 551 THz, que corresponde a luz de color turquesa.
Por lo tanto, el efecto fotoeléctrico depende del color, la misma placa de metal sodio no presenta efecto fotoeléctrico si se ilumina con luz verde, amarillo o rojo. Pero sí emite electrones cuando se ilumina con color azul o violeta.
En su momento, este hecho causó gran asombro en los científicos, que estaban convencidos de que si la intensidad de la luz incidente era lo suficientemente grande el fenómeno, se presentaría independientemente del color.
El potencial de frenado
Otro de los parámetros importantes es el potencial eléctrico necesario para detener el flujo de electrones. Ese potencial está relacionado directamente con la energía cinética de los electrones emitidos.
A su vez, los resultados de los experimentos iniciales mostraron que la energía de los electrones emitidos depende linealmente de la frecuencia de la luz, a partir de la frecuencia umbral, y no de la intensidad de la luz incidente.
De esta forma, tal como se dijo antes, los primeros experimentadores del efecto fotoeléctrico quedaron muy sorprendidos y no pudieron encontrar una explicación satisfactoria a este hecho.
La explicación de Einstein del efecto fotoeléctrico, y el fotón
Antes de 1905, los físicos estaban muy seguros que la luz tenía naturaleza ondulatoria. Es más, se sabía que la luz es una onda electromagnética capaz de propagarse libremente por el vacío, como lo hace la luz del Sol que llega hasta la Tierra. La vieja teoría corpuscular de la luz propuesta por Isaac Newton allá por los años 1600 había quedado atrás, ya que no podía explicar fenómenos típicamente ondulatorios, como la interferencia y difracción luminosa.
Einstein propuso en 1905 que la luz está compuesta por unas partículas sin masa, a las que llamó “fotones”.
Los fotones son partículas de luz cuya energía es proporcional a su frecuencia, es decir, a su color. Los fotones de color violeta son más energéticos que los azules, y estos a su vez más que los verdes y los verdes más energéticos que los amarillos y los amarillos más que los rojos.
La relación entre la energía de un fotón y su frecuencia es muy simple:
E = h∙f
Donde E es la energía, f es la frecuencia y h una constante de proporcionalidad llamada “constante de Planck”.
Esta constante había aparecido años antes para explicar la radiación luminosa de los cuerpos sometidos a altas temperaturas. En 1901, el físico Max Planck (1858-1947) concluyó que la radiación del “cuerpo negro” solo podía explicarse si el intercambio energético entre la onda electromagnética de la luz y el cuerpo se hacía en paquetes de energía E= h∙f, con “h” la constante de Planck.
Con esto en mente, Einstein propone que la luz incidente sobre la superficie metálica está compuesta por fotones, que transfieren toda su energía a los electrones no ligados del metal. Y cuando la energía ganada por los electrones es mayor o igual a la energía de atracción de los iones de la red cristalina, los electrones tienen velocidad suficiente para abandonar el metal.
Más todavía, Einstein propone que, a pesar de no tener masa, el fotón tiene cantidad de movimiento. ¿Cómo es posible? Se sabe que la cantidad de movimiento es el producto de la masa por la velocidad, pero el fotón no tiene masa.
Resulta que la cantidad de movimiento de un fotón es la constante de Planck dividida entre la longitud de onda del fotón. Einstein llega a esta conclusión a partir de su recién propuesta teoría de la relatividad especial. Años después, un famoso experimento para demostrar el efecto Compton confirmó más allá de toda duda este hecho.
Con la explicación del efecto fotoeléctrico nace la concepción actual de la mecánica cuántica, en el que toda partícula tiene asociada una onda y toda onda tiene asociada una partícula: la conocida dualidad onda-partícula.

Trabajo publicado en: Abr., 2021.